
活动内容收起
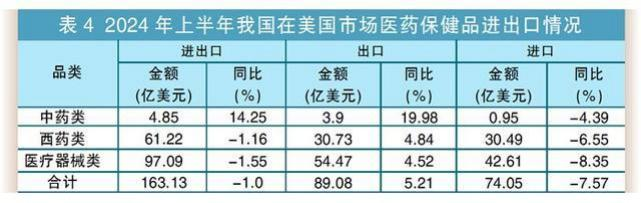
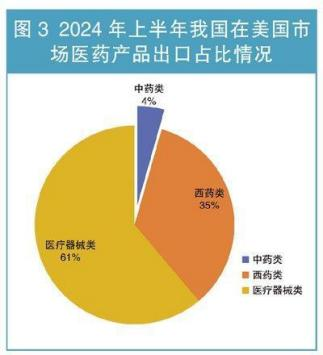
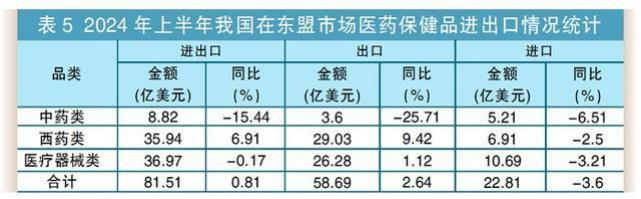
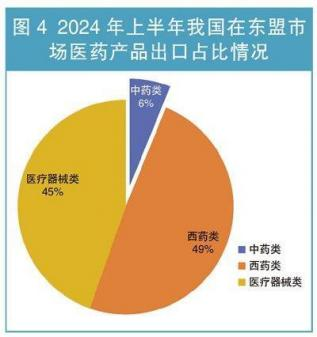
在全球化大潮下,中国医药企业正迎来前所未有的发展机遇与挑战。随着国家政策的支持与市场需求的增长,中国已成为世界第二大医药消费国,并逐步向世界制药强国迈进。然而,在这一过程中,如何保障药品质量和符合国际标准,成为每一家渴望拓展海外市场的企业必须面对的关键问题。据中国医药保健品进出口商会统计,2024 年上半年,中国在全球市场的医药产品进出口贸易额为 977.55 亿美元,同比下降 1.87%。其中,进口额 451.76 亿美元,同比下降 5.93%;出口额 525.79 亿美元,同比增长 1.91%。这预示着我国医药出口在经历大起大落之后,在今年上半年完成了常态化回归。具体产品和市场情况表现如下:
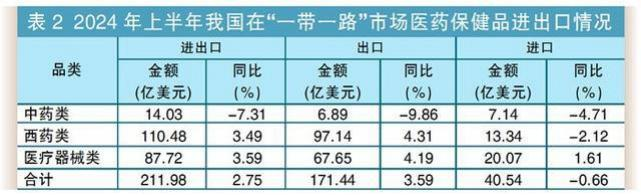
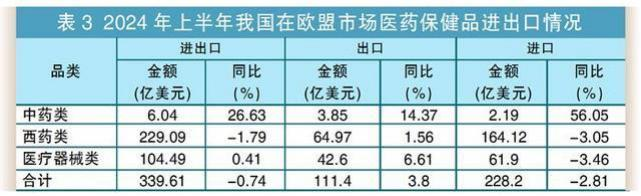
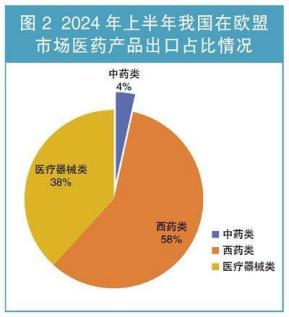
1、化药、医用耗材、诊断设备等产品出口增长较快 ,显示出我国医药出口产品结构进一步优化 ,为整体出口贡献了增量。 2、欧盟、美国市场复苏较快 ,分别增长3.8%和5.2% ,抵消了印度、 日韩市场的低迷 3、东盟市场平稳增长的趋势延续 ,市场多元化格局进一步深化。 4、受地缘、政治、军事政局和欧、美、印度原料药制造业回归等因素影响,全球医药产业链正在发动变化,市场多元化、出口结构优化是当前拉动我国医药出口增长的新动力。 1、面对如此内卷的国内市场,我们是否还要一个猛子扎进去而被浪潮淹没? 2、通过上面分析的内容,很显然出海是一个很好的选择。 3、面对这个机会,我们应该做些什么呢?我们应该知道些什么呢? 众所周知,FDA对于药品或原料药的检测标准与CDE在很多细分领域中有很多不同的要求。FDA作为一个在世界上被许多国家广泛认可的机构,其制定的药品标准以及审评的机制都相当的成熟和完整。而世界上的许多药品标准化组织如EMEA、WHO、ICH等,其标准都在向着FDA靠拢。而作为药品进入美国这一世界上最大市场的唯一途径,了解一下FDA对于新药和仿制药的要求和审批,对于制药企业有着相当的指导和现实意义。那么FDA和CDE到底有哪方面不同呢? 举一个简单的例子:细菌内毒素检测凝胶法对于仪器的要求方面,FDA要求对于检测结果的方法学方面带有自动审计追踪,如果没有了自动审计追踪,在相应的审评评分中就有适当的扣分。而目前纵观全世界的细菌内毒素凝胶测定仪,大部分均是使用手动凝胶以及肉眼观测数据审计。是否能够满足FDA的需求进而拿到加分项,就能为了细菌内毒素检测环节的关键点。 这样的例子还有很多,在此就不一个一个列举了。 为了顺应市场变化与趋势,拉动国内企业需求,带动国内企业业务多元化,西安药学会协同苏州蛋黄科技有限公司、北京乘风济海科技有限公司,于2025年3月初,在西安市共同举办【制剂及原料药出海产品质量控制与检测标准培训】。届时将特邀熟悉国内外药品研发、检验与申报要求的权威专家与企业,将其多年来在这方面积累的丰富经验和案例与大家分享。现将拟举办的【制剂及原料药出海产品质量控制与检测标准培训】相关信息发布如下: 一、主旨 1.聚焦国内药企关于产品出海业务的质量控制与实施 2.聚焦国内药企关于产品出海业务的检测标准与应用 3.聚焦相关检测与分析仪器的实际应用与效果展示 二、定位 1.提升国产出口药品的质量水平 2.引领或接轨国际检测标准与方法 3.展现国“芯”制造能力与档次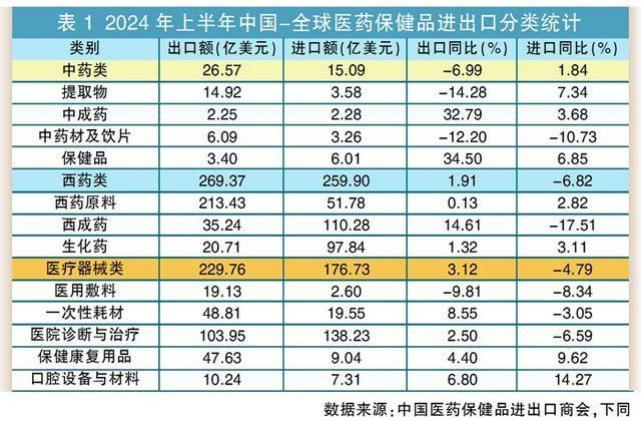

培训名称:制剂及原料药出海产品质量控制与检测标准培训
培训时间:2025年3月11日-3月12日
培训规模:100人
培训地点:西安宾馆 2层 延年阁
主办单位:西安药学会
承办单位:苏州蛋黄科技有限公司、北京乘风济海科技有限公司
(1)单敏 西安药学会秘书长 (2)刘海静 陕西省食品药品监督检验研究院院长 (3)高光 FDA驻中国区审评员 (4)李湛军 中国食品药品检定研究院理化室 原主任药师 (5)张启明 中国食品药品检定研究院化药室 原主任药师 (6)高华 中国食品药品检定研究院药理室 原主任药师 (7)魏世峰 北京罗诺强施医药技术研发中心有限公司 博士&董事长 (8)山东鲁抗医药股份有限公司 专家讲师 (9)湛江安度斯生物有限公司 专家讲师 (10)赵海山 天津市天大天发科技有限公司 总经理 (11)西安杨森制药有限公司 专家讲师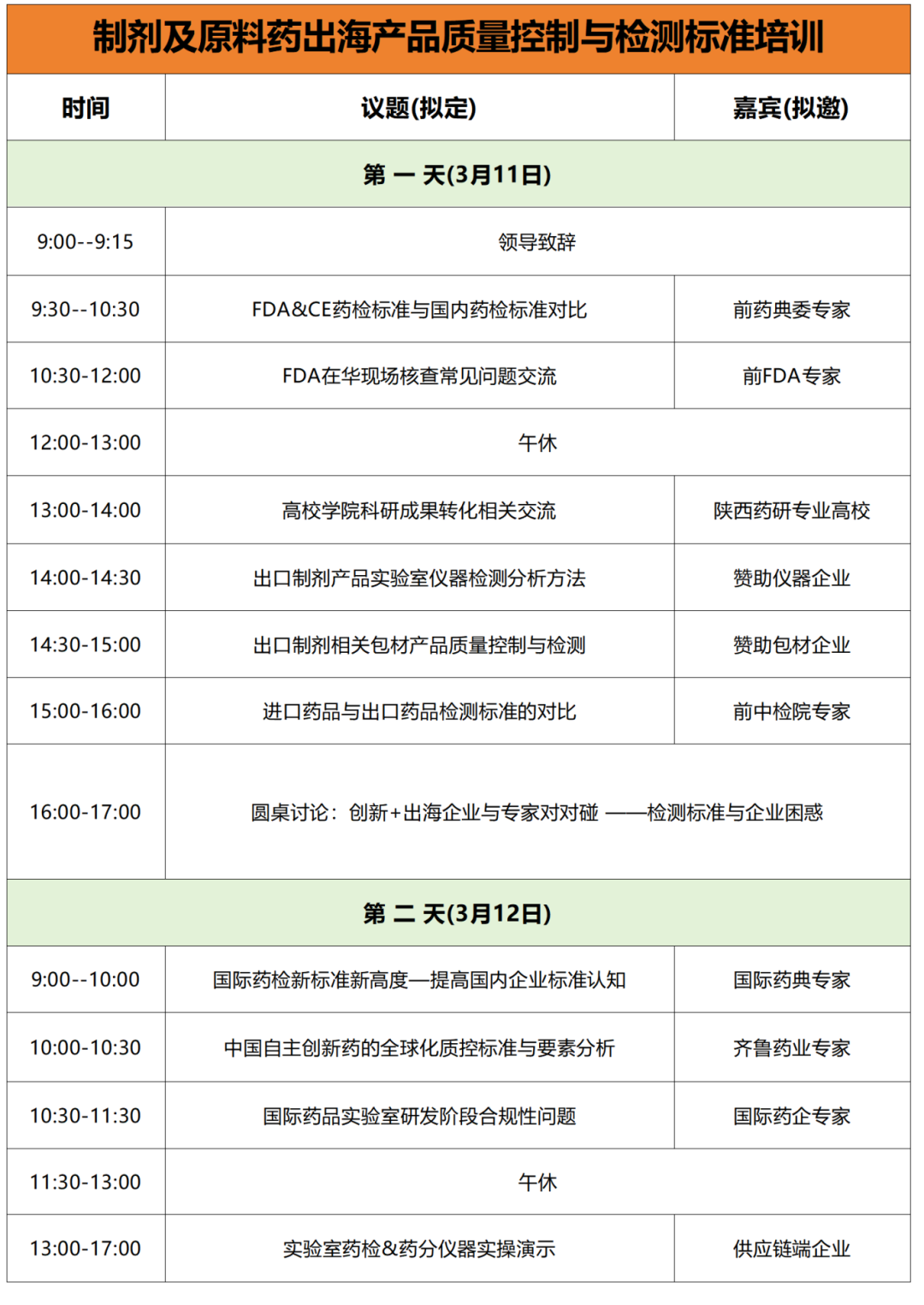
活动标签
报名须知
1、本活动具体服务及内容由主办方【北京蛋黄科技】提供,活动行仅提供票务技术支持,请仔细阅读活动内容后参与。
2、如在活动参与过程中遇到问题或纠纷,双方应友好协商沟通,也可联络活动行进行协助。







 北京蛋黄科技
北京蛋黄科技
















